Protein-, Zell-Engineering für biokatalytische Prozesse

Zur Bewältigung der Komplexität des natürlichen Stoffwechsels entstanden in der Evolution Biokatalysatoren mit herausragender Selektivität, die man heute für biotechnologische Prozesse nutzen kann. Die Möglichkeit, zwischen Molekülen zu unterscheiden oder von mehreren möglichen Reaktionsprodukten nur eines herzustellen, erlaubt oft die Einsparung von Reaktionsschritten und vereinfacht die Aufreinigung der Reaktionsprodukte. Es reduziert Kosten, Energiebedarf und die Entstehung von Abfall. Biokatalyse kann so einen erheblichen Beitrag zur Entwicklung umweltfreundlicher Prozesse fur die chemische und pharmazeutische Industrie leisten. Die Fähigkeit vieler Enzyme, nichtnatürliche Substrate umzusetzen, erlaubt ihren Einsatz zur Herstellung eines breiten Produktspektrums. Zudem katalysieren Enzyme viele Reaktionen, die für chemische Synthese zu anspruchsvoll wären. So können Enzyme selektiv Sauerstoffatome in unreaktive Moleküle einführen und stabile Bindungen wie Kohlenstoff-Kohlenstoff-Bindungen unter milden Reaktionsbedingungen selektiv brechen.
Wie bei allen katalytischen Prozessen stehen den Vorteilen der Aufwand und die Kosten der Herstellung des Katalysators gegenüber. Oft lässt sich ein Enzym mit seinen natürlichen Eigenschaften nicht einfach technisch einsetzen. Enzyme werden heute hauptsächlich im Bereich von Hochwertprodukten wie Pharmaka, Kosmetikprodukten und Lebensmittelzusätzen eingesetzt. Die Komplexität der Chemikalien und die hohen Anforderungen an die Produktreinheit führen bei chemischen Prozessen zu drastischen Abfallmengen und hohem Energiebedarf. Enzyme können hier die Nachhaltigkeit eines Prozesses deutlich verbessern. Die Biokatalyse ist in diesem Bereich oft die Methode der Wahl. Hochwertprodukte werden allerdings in relativ geringen Mengen hergestellt. Chemische Prozesse zur Herstellung von Massenprodukten produzieren generell weniger Abfall, sodass sich geringere Einsparungsmöglichkeiten ergeben. Dazu ist der Preis für Plattformchemikalien und Spezialchemikalien geringer, sodass Enzyme oft zu teuer sind. Bei der Nutzung erneuerbarer Rohstoffe in einer zukünftigen Bioökonomie kann die Biokatalyse einen wichtigen Beitrag leisten, da Enzyme zur Umsetzung biobasierter Stoffe hervorragend geeignet sind. Die Erhöhung der Effizienz biokatalytischer Prozesse zur Herstellung von biobasierten Massenprodukten und damit eine effektive Verbesserung der Kohlenstoffbilanz werden aktuell erforscht.
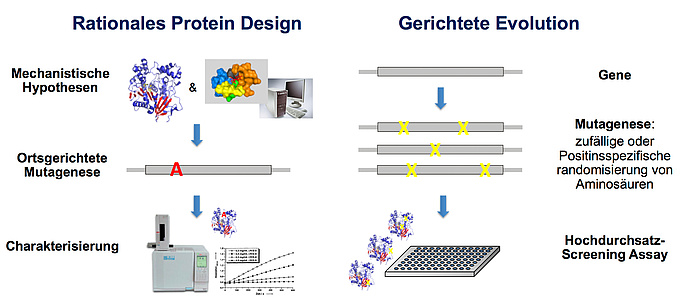
Verständnisbasiertes und daher „rationales“ Protein-Design und molekulare Optimierungsalgorithmen wie „gerichtete Evolution“ sind komplementäre Ansätze zur Optimierung von Enzymen für biotechnologische Anwendungen.
Optimierung von Enzymen
Biokatalysatoren wurden durch die Evolution fur ihre Funktion unter natürlichen Bedingungen angepasst, die sich oft erheblich von denen in industriellen Prozessen unterscheiden. Eine Optimierung von Biokatalysatoren kann entweder über eine Anpassung der Reaktionsbedingungen oder ein molekulares Design erfolgen. Bei Letzterem werden Mutationen in das Gen eingefügt, die in einer veränderten Zusammensetzung des Enzyms und so in neuen Eigenschaften resultieren. Das ermöglicht eine Aktivitatssteigerung, eine angepasste Selektivitat, eine höhere Stabilitat oder ein erweitertes Substratspektrum. Da das molekulare Verständnis oft keine akkuraten Vorhersagen über den Effekt einer Veränderung des Enzyms erlaubt, sind randomisierte Optimierungsverfahren wichtig. Molekulare Techniken führen über das Gen verteilt oder an ausgewählten Positionen eine Reihe verschiedener Aminosäuren ein. Die so entstehende kombinatorische Vielfalt wird in Hochdurchsatz-Screening-Assays durchmustert. Eine Kombination randomisierter Verfahren mit vorhandenem Wissen ist oft Schlüssel zum Erfolg. Rationales Proteindesign und gerichtete Evolution erlaubten so maßgeschneiderte Enzymvarianten.
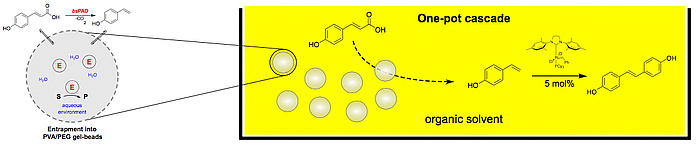
Die Verbindung chemischer und biokatalytischer Katalysatoren ermöglicht neue, umweltfreundliche biotechnologische Prozesse. Das Beispiel zeigt die Kombination einer enzymatischen Decarboxylierung mit der Olefin-Metathese zur Synthese biobasierter Antioxidantien. Die Abtrennung des Enzyms in Polymerkapseln ermöglichte eine Kompatibilität mit den Reaktionsbedingungen der chemischen Reaktion im organischen Lösemittel.
Enzyme als Bausteine
Da die meisten Enzyme in wassrigen Systemen und unter sehr moderaten Reaktionsbedingungen hervorragende Aktivitäten zeigen, können Enzyme zu Reaktionskaskaden zusammengestellt werden. Das ist ein Unterschied zu vielen chemischen Syntheserouten, in denen sich die Bedingungen der Reaktionsschritte oft drastisch unterscheiden und Kompatibilität nicht erreichbar ist. Die Aufarbeitung der intermediaren Reaktionsprodukte in den Kaskadenreaktionen ist so nicht mehr nötig, was die Prozesse effizienter gestaltet. Ein weiterer Ansatz ist die Kombination von Enzymen mit chemischen Katalysatoren. Das erlaubt die Kombination der synthetischen Stärken beider Gebiete. Enzyme aus verschiedenen Organismen unterscheiden sich oft in ihren optimalen Reaktionsbedingungen und katalysieren oft die Umsetzung der Reaktionspartner von anderen Reaktionsschritten der Kaskade. Eine erfolgreiche Etablierung und Skalierung von multi-katalytischen Reaktionskaskaden ist daher erheblich anspruchsvoller als bei Einzelreaktionen. Der Schlüssel liegt hier im erfolgreichen Zusammenspiel molekularer Ansätze wie Protein- und Zell-Engineering und verfahrenstechnischer Methoden. Trotz dieser Schwierigkeiten zeichnet sich ab, dass die Stärke von Biokatalysatoren in ihrer einfachen Anknüpfbarkeit an andere Reaktionen liegt. Das immense metabolische Potenzial von Reaktionskaskaden in lebenden Zellen und zellfreien Systemen ist nicht ausgeschöpft. Beispiele wie die Kombination von Enzymen mit chemischen Katalysatoren in Tandemreaktionen oder die Anknüpfung von Enzymen an die natürliche Photosynthese als Energiequelle unterstreichen das synthetische Potenzial der Biokatalyse. Die Komplexität der Reaktionssysteme erfordert aber eine stärkere interdisziplinare Integration von molekularen Methoden und Prozesstechnik. Protein- Engineering ist ein effizientes Werkzeug, um Enzyme im Hinblick auf Aktivität, Selektivitat und Stabilität für den Einsatz in Kaskadenreaktionen zu optimieren.
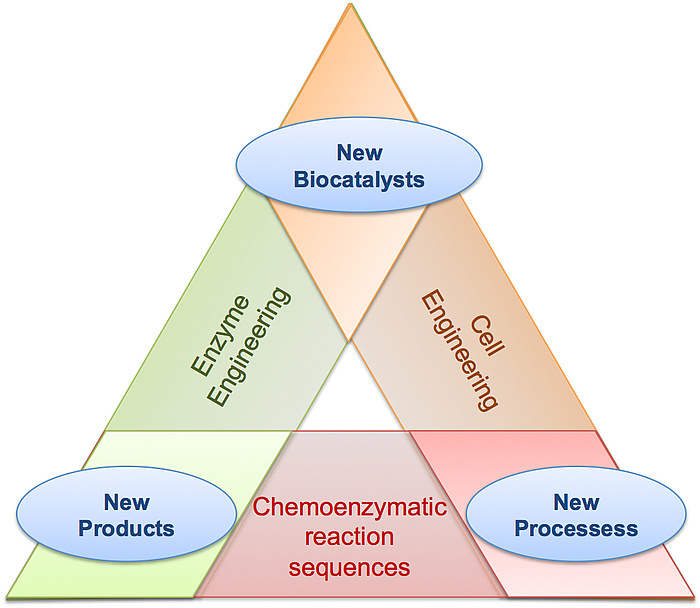
Forschung an der Arbeitsgruppe für Biokatalyse und Enzym Engineering am Institut für Molekulare Biotechnologie.
Dieses Forschungsgebiet ist im FoE „Human & Biotechnology“ verankert, einem der fünf Stärkefelder der TU Graz.



